Salutations les habitants de notre site!
D'année en année, la production de pétrole devient de plus en plus complexe et le carburant qui en découle devient de plus en plus cher. Dans les pays de l'UE, ils menacent généralement de ne plus produire de moteurs à essence, ils veulent remplacer tous les véhicules par des voitures électriques. Mais les batteries au lithium sont encore loin d'être idéales, et d'ailleurs, elles ne sont pas du tout pressées de devenir idéales du tout. Dans le meilleur des cas, sur une seule charge d'une batterie au lithium, il sera possible de couvrir une distance maximale de 700 km, après quoi vous devrez charger la batterie pendant environ une semaine, et si vous utilisez une prise ordinaire pour la charge, cela prend généralement beaucoup de temps. Et vous imaginez simplement ce qui se passera si tout le monde commence à charger constamment ses voitures électriques, quelles seront les énormes charges sur le réseau électrique et quelle tension s'écoulera. En général, l'avenir des batteries au lithium est encore assez vague et chaque année de plus en plus de recherches sont consacrées à la recherche de nouvelles options de batteries.
Comme vous le savez, le métal le plus énergivore est l'aluminium. Déjà à notre époque sur certains prototypes de batteries en aluminium, vous pouvez parcourir environ 2000 km sans recharger, et recharger ce type de batterie ne prend que 15 minutes, après quoi vous pouvez aller plus loin pendant environ 2000 km.
La recharge des batteries en aluminium diffère de la recharge des batteries au lithium. Néanmoins, il n'y a rien de compliqué, il vous suffit d'insérer un nouvel aluminium, de verser l'électrolyte et de verser un nouvel électrolyte, tout est essentiellement le même que l'essence une voiture, seulement c'est une voiture électrique, et il n'y a pas de charges sur le réseau électrique. De plus, vous n'avez pas besoin de produire un grand nombre de prises avec des fils avec une section transversale énorme pour charger toutes ces voitures électriques.
Mais tout n'est pas si doux ici. L'électricité à partir de l'aluminium n'est pas du tout aussi simple que nous le souhaiterions. Voyons d'abord quel est le principe de la batterie aluminium-air.
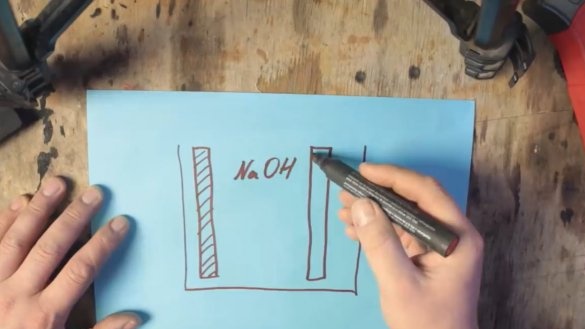
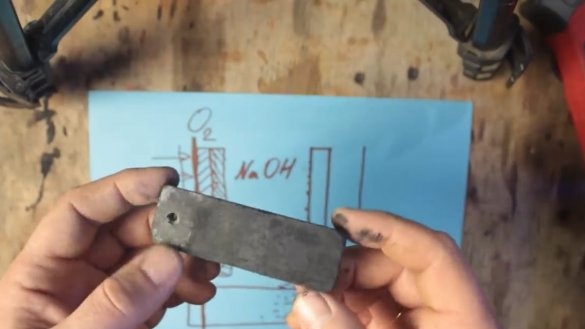
Pour qu'une telle batterie commence à fonctionner, 2 électrodes seront nécessaires: une naturellement en aluminium et la seconde en graphite. Ces deux électrodes sont dans une solution électrolytique.
Le sel (NaCl) peut être utilisé comme électrolyte, mais avec lui, vous pouvez augmenter la tension à environ 0,7 V. La tension de l'électrolyte alcalin (NaOH) peut déjà être augmentée à environ 1V.
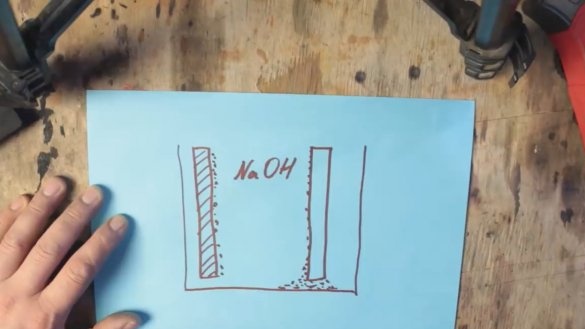
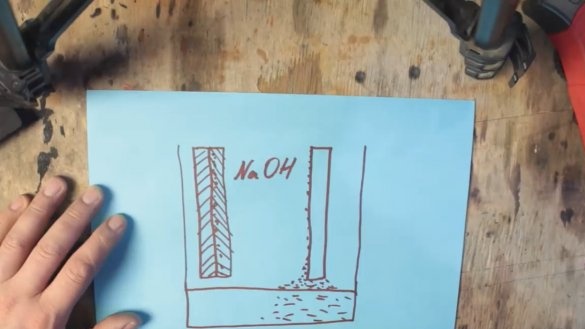
Au cours de la réaction chimique, l'aluminium est recouvert d'une couche d'hydroxyde d'aluminium (Al (OH) 3), qui s'enfonce progressivement au fond du réservoir. Et à la surface de l'électrode en graphite, des bulles d'hydrogène se forment, ce qui entraîne à son tour une augmentation de la résistance et une chute de tension, ce processus est appelé polarisation.
Le premier problème avec la précipitation de l'hydroxyde d'aluminium peut être éliminé en augmentant simplement la capacité où le produit usé se déposera, mais le deuxième problème peut être résolu par une masse dépolarisante à base d'oxyde de manganèse, qui se transformera en hydroxyde de manganèse pendant le fonctionnement.
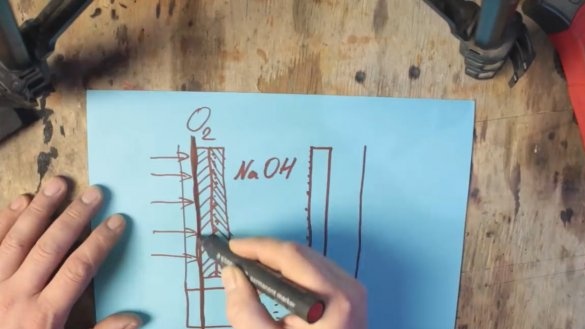
En fait, nous avons obtenu une pile alcaline ordinaire, mais seulement une très grande. Mais un nouveau problème se pose. Le fait est que l'oxyde de manganèse est également consommé et qu'il devra également être changé. Et nous devons nous assurer que seul l'aluminium est dépensé. Pour ce faire, prenez de l'oxygène de l'air ambiant. C'est là que commence la batterie aluminium-air. L'une des parois doit simplement être remplacée par une membrane perméable aux gaz et l'électrode en graphite doit être remplacée par un mélange de graphite et d'oxyde de manganèse avec des nanoparticules de platine ou d'argent.
L'oxyde de manganèse avec des nanoparticules de métaux nobles ne réagit pas, mais agit comme un catalyseur, grâce auquel l'hydrogène de l'électrolyte est oxydé par l'oxygène de l'air.
La technologie de production d'oxyde de manganèse avec inclusions de nanoparticules d'argent n'est en principe pas compliquée et peut être expérimentée dans des conditions artisanales. Mais dans cet article, nous verrons comment faire l'option la plus économique pour une batterie qui reçoit de l'énergie de l'aluminium. Les instructions suivantes sont extraites de la chaîne de télévision Fiery YouTube. Plus de détails dans la vidéo originale de l'auteur:
La version à budget maximum du graphite est des inserts de contact d'été pour les trolleybus. Ils peuvent être trouvés absolument gratuitement aux derniers arrêts de trolleybus, ou vous pouvez les acheter, ils ne sont pas chers, l'auteur les a trouvés en vente à 22 roubles chacun.
Ensuite, nous avons besoin d'un alcali. Voici un outil pour nettoyer les tuyaux dans sa composition contient cent pour cent d'alcali de sodium.
Pour démarrer la réaction alcaline, il nous faut juste un peu, 1 g d'alcali pour 0,5 l d'eau suffira.
Tout d'abord, vérifions si une électrode en graphite est vraiment nécessaire dans cette batterie. Pour l'expérience, prenons cette électrode en acier inoxydable.
Maintenant, nous mettons la plaque d'aluminium et l'électrode en acier inoxydable dans l'alcali, connectons le multimètre et voyons combien de volts il s'avère.
Comme vous pouvez le voir, il s'est avéré être d'environ 1,4 V. Vérifions maintenant le courant de court-circuit.
Le courant de court-circuit s'est avéré de l'ordre de 20mA. Quelles conclusions peuvent être tirées: théoriquement dans des conditions extrêmes, il est possible d'assembler une batterie de tasses en acier inoxydable et une feuille d'aluminium.
Ensuite, nous aurons une électrode en cuivre en cuivre électrique.
Comme nous pouvons l'observer, la tension s'est avérée être légèrement supérieure à 1,4 V, mais le courant de court-circuit était d'abord élevé, mais il a commencé à s'affaisser assez rapidement et le cuivre a également commencé à se recouvrir d'un revêtement sombre, cet effet étant probablement dû à des impuretés dans l'eau, car l'eau Dans cette expérience, l'auteur a pris un robinet d'un robinet.
Immergez maintenant l'électrode en graphite dans la solution d'électrolyte.
Avec cette électrode, une tension de 1,3 V a été obtenue, le courant de court-circuit s'est arrêté aux alentours de 17 mA. À première vue, il semble que l'électrode en acier inoxydable soit plus efficace, mais la surface de l'électrode en acier inoxydable est plus grande, donc on ne sait pas encore quel graphite ou acier inoxydable est le meilleur.
Étant donné que le graphite a une résistance assez importante, vous devez en quelque sorte y faire face. Il est nécessaire de fabriquer des électrodes à partir d'un matériau bien conducteur et le graphite ne doit être qu'à sa surface.Il a été décidé de percer le graphite et, dans les trous résultants, de couper le filetage des boulons m6.
Le résultat est une électrode en acier avec une coque en graphite.
La résistance du graphite non percé est d'environ 4,5 Ohms, mais celle du graphite foré est d'environ 1,7 Ohms.
Sur le visage, une diminution de la résistance et, par conséquent, l'efficacité de la structure vont augmenter. Dans d'autres expériences, nous utiliserons de l'eau distillée.
La première expérience avec un électrolyte, dans lequel 4 g d'alcali pour 1 litre d'eau.
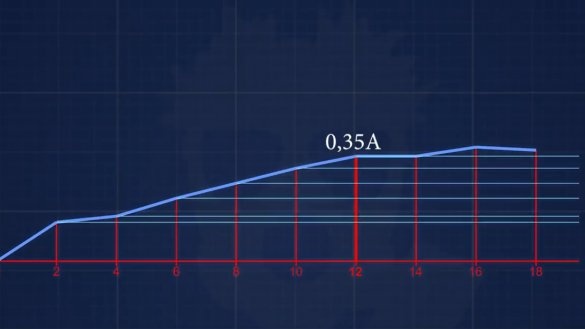
Le courant de court-circuit s'est avéré 150mA. L'électrolyte suivant a une concentration de 6 g d'alcali pour 1 litre. Eh bien et ainsi de suite, à chaque fois nous augmenterons la concentration de 2 g jusqu'à atteindre une concentration à laquelle le courant n'augmentera pas.
Même si une batterie aussi simple n'a pas une grande efficacité de courant, mais une telle batterie peut fonctionner très longtemps et tout aluminium peut être utilisé comme électrodes, qui peuvent facilement être fondues en électrodes de n'importe quelle forme, par exemple, des canettes en aluminium diverses boissons alcoolisées et non alcoolisées, feuille de chocolat, etc.
En conséquence, après toutes les expériences avec différentes concentrations d'électrolyte, il devient clair qu'avec cette conception de la batterie, cela n'a aucun sens d'ajouter plus de 12 g d'alcali à 1 litre d'eau, c'est-à-dire que nous obtenons environ 1% de solution.
Ensuite, l'auteur a assemblé un autre clip, composé de 3 électrodes.
Deux batteries donnent une tension plus élevée et moins de perte, donc le résultat est meilleur.
Prenons maintenant un seau d'électrolyte, un gros morceau d'aluminium et 2 électrodes en acier inoxydable.
Dans un seau, une concentration en électrolyte de 10g / 1l. Courant de crête de 1,3 A, il s'est affaissé à 520 mA. Avec toute l'énorme surface de l'acier inoxydable, il ne se comparait pas au graphite, car il s'avérait être 600 mA avec le graphite. Soit dit en passant, l'hydrogène est libéré pendant la réaction, qui peut également être collecté et utilisé comme source d'énergie. Bref, il y a de la place pour grandir. C'est tout pour l'instant. Merci de votre attention. A très bientôt!